

Profa. Dra. Marília W. Mancini
Coordenadora do Laboratório de Biofotônica – Instituto Nupen
Para citar este texto:
As técnicas para utilização da terapia laser de baixa intensidade (LLLT - low level laser therapy) ou fotobiomodulação (PBM - photobiomodulation) consistem em métodos terapêuticos não-invasivos com ação de modulação da inflamação, reparo tecidual e analgesia [1,2]. Dentre entre outros efeitos terapêuticos adicionais proporcionados pela fotobiomodulação sistêmica (técnica ILIB), tais como, efeitos de vasodilatação e consequente redução de pressão arterial, anti-hipóxico, antioxidativo, regulação das taxas de glicose, colesterol e lipoproteínas de baixa densidade (colesterol LDL), além de estabilização do sistema imunológico e fotorreativação da enzima superóxido dismutase (SOD), promovendo o restabelecimento do sistema antioxidante endógeno, importante no tratamento de processos inflamatórios agudos e crônicos e na prevenção de doenças sistêmicas, conforme amplamente investigado na literatura, empregando luz laser com
emissão típica na faixa de comprimentos de onda de 400 nm a 1070 nm [1-5], e potências ópticas de saída na faixa de 1,0 mW até 1000 mW [1-3] (a depender do tamanho do spot do laser ou LED), em parâmetros dosimétricos específicos para as diferentes ações pretendidas, dose-dependentes.
A faixa de comprimentos de onda supracitada empregada para fotobiomodulação se refere ao espectro de absorção do fotorreceptor celular citocromo c oxidase (CCO), presente na mitocôndria [1,6,7] a partir de quatro grupos metálicos (Fe e Cu) ativos, a saber, os grupos férricos (heme a e heme a3) e cúpricos (CuA e CuB) [6]. A Figura 1 apresenta uma representação do CCO e de seus 4 grupos absorvedores.
A absorção da luz pelo CCO na região do espectro visível (400-760 nm) é dominada pelo grupo heme a, com máximo em torno de 598 nm (banda Q), e sendo a estrutura em 655 nm associada ao centro binuclear a3/CuB totalmente oxidado. Em especial, a banda Soret (situada entre 400-450 nm, com pico em 423 nm) é devida aos grupos hemes a e a3 [8].
Essa região associada à banda Soret concerne a emissão dos modelos e-light – DMC, com aparelhos de cluster de LEDs emitindo em 410 nm (violeta) e 450 nm (azul) referente aos modelos e-light V e e-light B, respectivamente, por exemplo.
O aparelho e-light LEDs âmbar, modelo e-light A (590 nm) tem emissão ressonante com o pico da banda Q com máximo situado em 598 nm.
Em especial, a janela terapêutica (600-1000 nm) abarcando as subfaixas do vermelho (640-760 nm) e infravermelho (760-1000 nm) se justificam pela maior profundidade de penetração tecidual (dada pelo inverso do coeficiente de absorção reduzido tecidual, levando em conta a contribuição dos principais cromóforos do tecido biológico, incluindo cromóforos concorrentes ao CCO, a saber, a melanina, a hemoglobina (absorção no azul e no verde) e a água (picos de absorção no infravermelho, a partir de 980 nm até o máximo em 3.000 nm), justificando os comprimentos de onda de operação dos equipamentos da Família Therapy (aparelhos Therapy XT, Therapy EC, Therapy Plus e Therapy ACP) – DMC (660 nm e 808 nm) e Therapy ILIB-R (660 nm), do aparelho e-lib (660 nm), e dos equipamentos e-light modelos RL (660 nm), IRL (660 nm e 808 nm), IL (808 nm). Os modelos e-light com LEDs emitem no vermelho em 650 nm (modelo R) e no infravermelho próximo (modelo I) em 850 nm.
A região espectral de 700-980 nm é dominada pela contribuição do CuA. A banda situada entre 715 e 920 nm é associada com o centro binuclear heme a3/CuB [6] (808 nm – família Therapy, e-light IL e 850 nm no e-light I).
Acerca da família de clusters de LEDs e lasers de diodo, e-light (link) da DMC, foram citados no presente texto os modelos de clusters de LEDs envolvendo um único comprimento de emissão. Contudo modelos duais e tríades, ou seja, com dois ou três comprimentos de onda de emissão são também disponíveis.
A Figura 2, a seguir, apresenta os espectros de absorção do citocromo c oxidase (CCO) (em suas formas oxidada e totalmente reduzida – curvas em preto e vermelho, respectivamente Fig. 1 (adaptado de Masson 2014) [6].
Figura 2 – Figura 1 de Masson et al. 2014. Características ópticas do citocromo c oxidase (CCC) nas formas oxidada (preto) e reduzida (vermelho) nas bandas Soret, VIS (visível) e NIR (infravermelho próximo). Detalhes da solução utilizada no artigo citado. O gráfico principal adquirido a solução 4,9 mM. Os gráficos menores (insets) mostrando o espectro nas regiões 500-750 nm e 600-1.000 nm obtidos a partir de uma concentração 5 x maior. O espectro da enzima oxidada tem máximos da banda Soret em 423 nm e 598 nm, respectivamente. Os coeficientes de extinção são mostrados na Tabela 1 do artigo referido.
A partir do processo de absorção dos fótons do laser pelo CCO mitocondrial, através de seus centros absorvedores, processos fotoquímicos no interior da célula e na membrana celular originam os efeitos terapêuticos supracitados, apresentados na larga literatura a respeito dos mecanismos de ação da LLLT ou PBM.
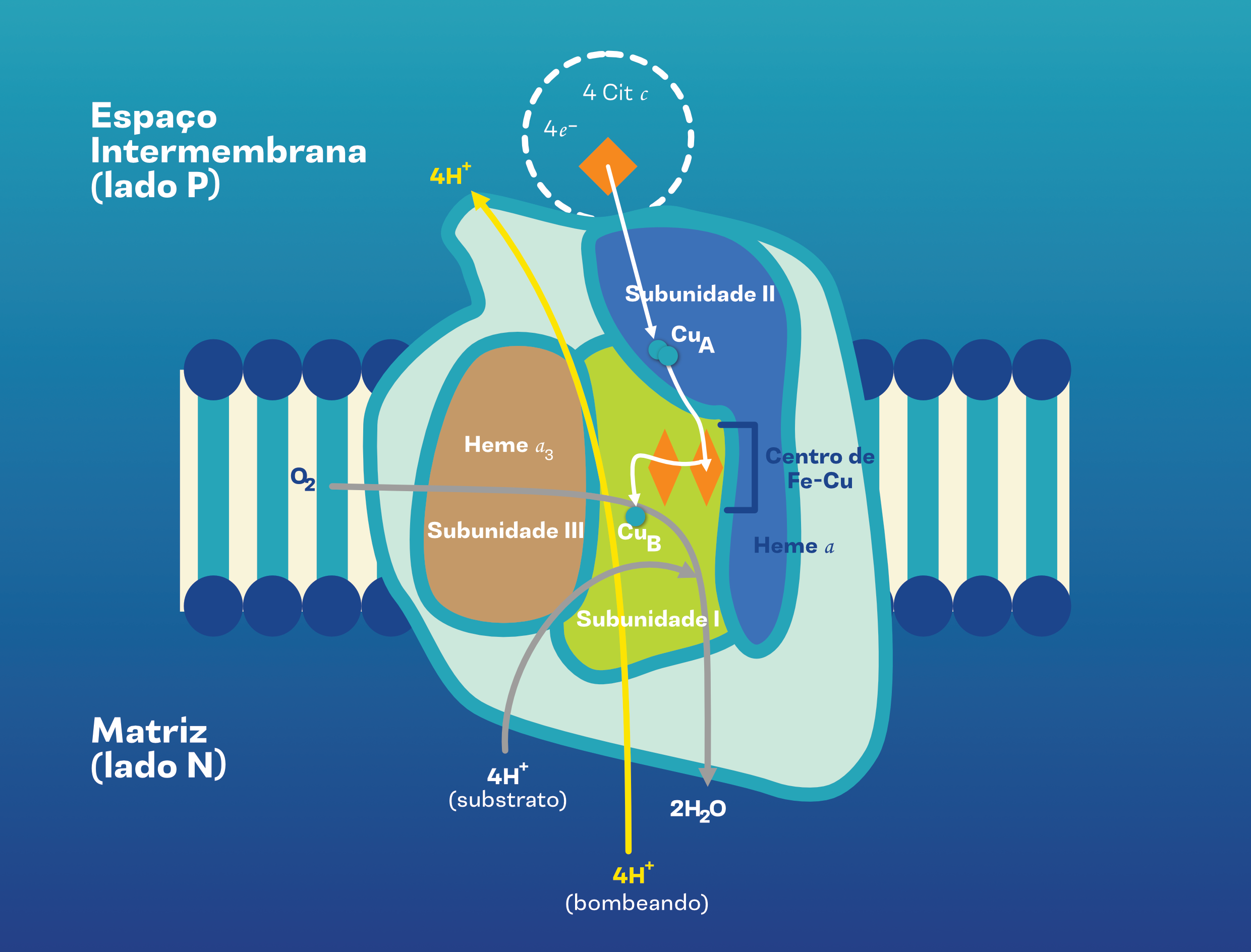
Fig. 1. Representação esquemática do cromóforo citocromo c oxidase (CCO) e seus quatro centros absorvedores: grupos férricos (heme a e heme a3) e cúpricos (CuA e CuB).
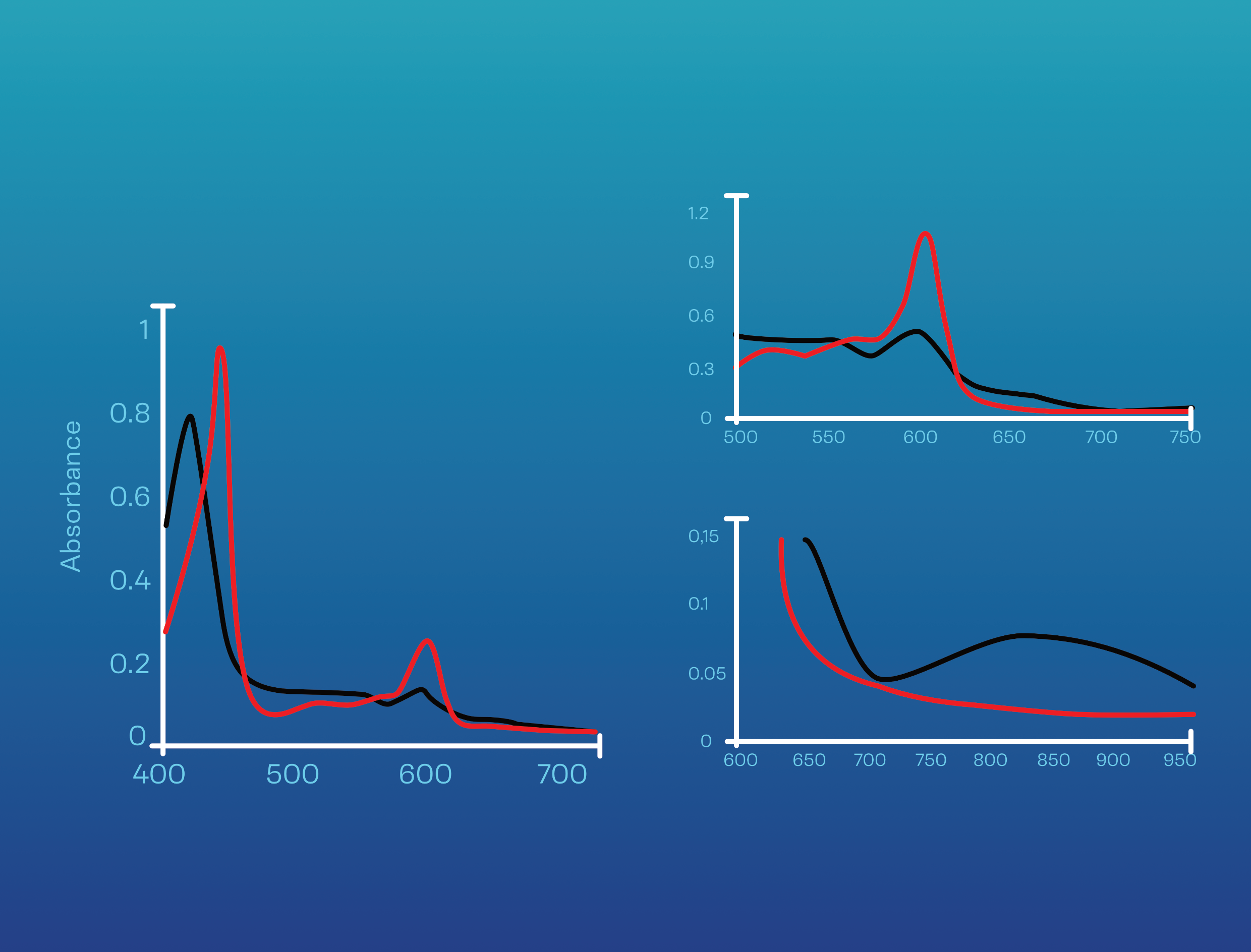
Fig. 2. Espectro de absorção do citocromo c oxidase (CCO) (em suas formas oxidada – curva em preto e totalmente reduzida – curva em vermelho) – absorbância x comprimento de onda (a) (adaptado de Masson 2014) [6].
Referências:
[1] Chung H, Dai T, Sharma SK, Huang YY, Carroll JD, Hamblin MR. The nuts and bolts of low-level laser (light) therapy. Ann Biomed Eng. 2012 Feb;40(2):516-33. doi: 10.1007/s10439-011-0454-7.
[2] Capaldi RA, Malatesta F, Darley-Usmar VM. Structure of cytochrome c oxidase. Biochim Biophys Acta. 1983; 726:135–148.
[3] Castano AP, Dai T, Yaroslavsky I, Cohen R, Apruzzese WA, Smotrich MH, Hamblin MR. Low-level laser therapy for zymosan-induced arthritis in rats: importance of illumination time.
[4] Sterczała, B.; Grzech-Leśniak, K.; Michel, O.; Trzeciakowski, W.; Dominiak, M.; Jurczyszyn, K. Assessment of Human Gingival Fibroblast Proliferation after Laser Stimulation In Vitro Using Different Laser Types and Wavelengths (1064, 980, 635, 450, and 405 nm) -Preliminary Report. J. Pers. Med. 2021, 11, 98. https://doi.org/10.3390/jpm11020098
[5] Prado, T.P.; Zanchetta, F.C.; Barbieri, B.; Aparecido, C.; Melo Lima, M.H.; Araujo, E.P. Photobiomodulation with Blue Light on Wound Healing: A Scoping Review. Life 2023, 13, 575. https://doi.org/10.3390/life13020575
[6] Mason M.G., Nicholls P., Cooper C.E., Re-evaluation of the near infrared spectra of mitochondrial cytochrome c oxidase: Implications for non invasive in vivo monitoring of tissues,
Biochimica et Biophysica Acta (BBA) – Bioenergetics 2014, 1837, 11, 1882-1891. https://doi.org/10.1016/j.bbabio.2014.08.005.
[7] Karu T.I., Pyatibrat L.V. and Afanasyeva N.I., A Novel Mitochondrial Signaling Pathway Activated by Visible-to-near Infrared Radiation, Photochemistry and Photobiology, 2004, 80: 366–372.
[8] Diuba, A.V., Vygodina T.V., Azarkina N.V., Arutyunyan M.A., Soulimane T, Vos. M.H., Konstantinov A.A. Individual heme a and heme a3 contributions to the Soret absorption spectrum of the reduced bovine cytochrome c oxidase, Biochimica et Biophysica Acta (BBA) 2023, Bioenergetics 1864, Issue 2, 1, 14893. https://doi.org/10.1016/j.bbabio.2022.148937