El término blanqueamiento dental se resume químicamente a una reacción donde ocurre quiebra de moléculas cromóforas presentes en agrupamientos orgánicos e inorgánicos de la estructura dental. Durante el blanqueamiento, los pigmentos, constituidos por moléculas carbónicas insaturadas van saturándose por la acción local de radicales libres. Así, las dobles ligaciones entra los carbonos son deshechas modificando el espectro de absorción de aquellas moléculas, posibilitando así, una mayor reflexión de la luz, y consecuentemente, una estructura dental más clara, La generación de los radicales libres puede ser realizada con el peróxido de hidrógeno o con la carbamida que, por ser inestables producen los radicales libres que proporcionarán la reacción de blanqueamiento dental [1].
Con la idea de provocar la aceleración de la reacción química diferentes métodos son utilizados en el procedimiento de blanqueamiento dental. En entre estos podemos citar: modificación de pH; aumento de la temperatura a través de la vibración molecular (calor); y catalizadores químicos. En este módulo vamos a ilustrar las diferentes acciones de la fotocatálisis en la aceleración de la reacción para obtener el blanqueamiento dental.
A fin de comprender cómo la luz es capaz de producir fotocatálisis, necesitamos resumidamente entender qué es la luz. La luz es una forma de energía electromagnética cuyo ancho de onda se extiende desde la radiación gama hasta la radiación infrarroja, invisibles al ojo humano. La parte visible del espectro está comprendida en un ínfimo intervalo entre el color violeta y el color rojo (Fig 1).
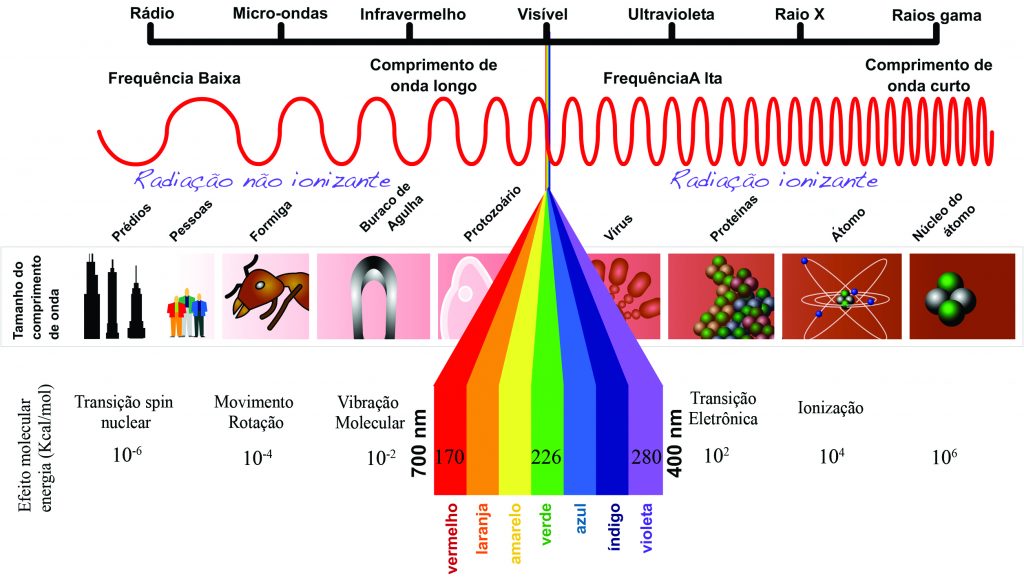
Figura 1 – Espectro eletromagnético.
La figura 1 ilustra las diferentes irradiaciones con sus respectivas características físicas. Así, por presentar energía limitada, la luz visible necesita una molécula capaz de absorberla para generar catálisis, y consecuentemente que ocurra aumento de temperatura. Es como exponer un material de color negro o blanco a la energía del sol. Con seguridad tendremos un aumento de temperatura en la superficie oscura que absorbe la luz, mientras que la superficie clara, reflejando la misma, no calentará. Por cuenta de esto, los agentes blanqueadores más efectivos para ser catalizados por la luz son aquellos que poseen colores complementarios. El color de la fuente emisora de luz, en la mayoría de los instrumentos es emitida por “LEDs – Light Emission Diodes” azules, o sea, si estamos haciendo un blanqueamiento con fuente de luz azul debemos utilizar colores en el agente blanqueador que absorben el azul, por ejemplo, amarillo, rojo, naranja, violeta. El calentamiento en la superficie del gel de blanqueamiento proporciona, por la leyes de la cinética química de Arrhenius, un aumento de la velocidad de la reacción de catálisis, liberando así más rápidamente los radicales libres que serán responsables por el blanqueamiento dental. Esta reacción es conocida como foto-termo catalítica [2]. Por otro lado, la radiación infrarroja emitida por láseres de baja potencia es capaz de proporcionar mayor vibración en diferentes moléculas. Este aumento de la vibración genera calor en la superficie irradiada.
Así, tenemos en el blanqueamiento dental la posibilidad de proporcionar dos tipos de fotocatálisis: una dependiente de la absorción de la energía luminosa por colorantes agregados en los agentes blanqueadores y o otra por catálisis directa utilizando la radiación infrarroja.
Diferentes investigaciones evidencian resultados semejantes en efectividad de blanqueamiento, sin embargo difieren estadísticamente en relación al tiempo del procedimiento, sin embargo difieren estadísticamente en relación al tiempo del procedimiento en el cual, con fuente de luz proporciona una reacción al tiempo del foto-catalización [3, 4]. En la figura 2 se observa que la tasa de blanqueamiento final es la misma cundo la sustancia es sometida a fuente de luz, o no. Sin embargo, es evidente que con la fuente de luz el resultado ocurre más rápidamente beneficiando así el desempeño del procedimiento de blanqueamiento dental.

Figura 2 – Gráfico demostrativo de la aceleración del procedimiento de blanqueamiento con fuentes de luz.
Los nuevos conceptos del blanqueamiento dental con fuente de luz propician no solo una disminución del tiempo del procedimiento, pero también la posibilidad de utilizar concentraciones más bajas del agente blanqueador obteniendo menor posibilidad de sensibilidad, y mayor seguridad para el paciente, según vemos por la figura 3.
Con el advenimiento de la nanotecnología nuevos conceptos de foto-catalización fueron desarrollados, entro los cuales, la incorporación de nanomoléculas fotosensibles en agentes blanqueadores posibilitó reacciones de catálisis directa utilizando la luz visible, sin la necesidad de aumento de la temperatura. Como vimos, toda esta tecnología propició la disminución de la concentración de agentes blanqueadores debido a mayor eficiencia de la reacción de liberación de radicales libres. Ejemplo de este concepto es la incorporación de dióxido de titanio en los agentes blanqueadores [5].
Por fin, vimos que la foto-catalización proporciona tanto la posibilidad de aumentar la velocidad de la reacción del blanqueamiento dental, así como viabiliza la disminución de concentración de los agentes blanqueadores, disminuyendo así, significativamente el índice de sensibilidad de los pacientes (Fig. 3) [4].
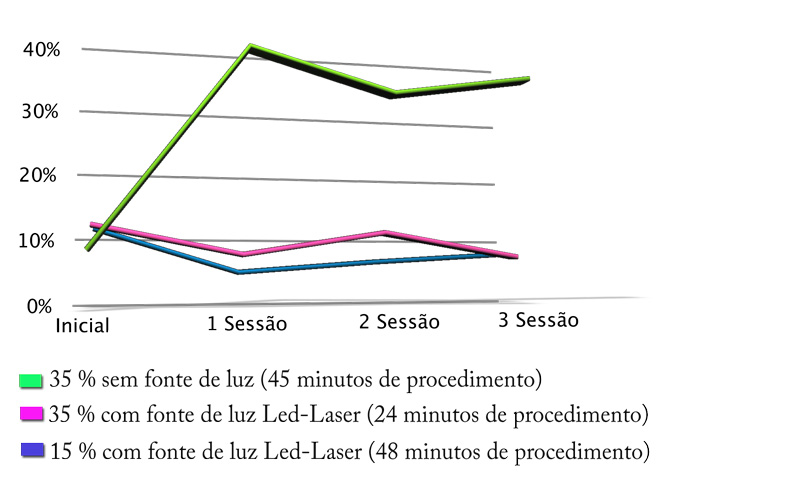
Figura 3 – Índice de sensibilidad en función concentración del blanqueador, exposición o no fuentes de luz y tiempo de procedimiento.
La búsqueda por una odontología mínimamente invasiva no hace pensar en un cambio en los abordajes estéticos a fin de proporcionar una mayor seguridad para los pacientes. El blanqueamiento dental debe ser comprendido como un procedimiento restaurativo estético conservador buscando la coloración natural de las estructuras dentales que son únicas para cada individuo. Y para esto debemos cada vez más preocuparnos con la indicación de procedimientos personalizados para cada paciente, disminuyendo el tiempo del procedimiento, o la concentración del agente blanqueador utilizando, por ejemplo, la tecnología de LASERs y LEDs como fuentes de luz.
Hermes Pretel*, CD, Msc., Dr.
* Maestrazgo y Doctorado – Ciencias Odontológicas – Facultad de Odontología de Araraquara – UNESP.



